2021年12月24日にラゲブリオカプセル(一般名:モヌルピラビル)が特例承認されました。
以前に経口コロナ治療薬 モルヌピラビルについて調べてみました | りんブログ (lynn-pharma.com)でもご紹介しましたが、添付文書や審議結果報告書から、さらに分かった部分もあったので紹介します。
ラゲブリオカプセルについて
薬効薬理
薬効薬理について添付文書に次の記載があります。
- 作用機序:モルヌピラビルはプロドラッグであり、NHC(N-ヒドロキシシチジン)に代謝され細胞内に取り込まれた後、活性型であるNHC-TPにリン酸化される。NHC-TPがウイルス由来RNA依存性RNAポリメラーゼによりウイルスRNAに取り込まれた結果、ウイルスゲノムのエラー頻度が増加し、ウイルスの増殖が阻害される。
- In vitro抗ウイルス作用:NHCはVero E6細胞を用いた細胞培養系でSARS-CoV-2に対して抗ウイルス作用を示し、50%有効濃度(EC50値)は0.78~2.03μmol/Lであった。NHCはSARS-CoV-2の従来株(USA-WA1/2020株)、並びにその変異株であるB.1.1.7(α株)、B.1.351(β株)、P.1(γ株)及びB.1.617.2(δ株)に対して同程度の抗ウイルス作用を示し、EC50値はそれぞれ1.41、1.59、1.77、1.32及び1.68μmol/Lであった。
- In vivo抗ウイルス作用:SARS-CoV-2感染マウス、ハムスター及びフェレットモデルを用いてモルヌピラビルの抗ウイルス作用を確認した。マウスでは、モルヌピラビルはウイルスを接種した移植ヒト肺組織でのSARS-CoV-2の感染性ウイルス量を減少させた。SARS-CoV-2感染フェレットモデルでは、モルヌピラビルは上気道でのSARS-CoV-2の感染性ウイルス量を減少させ、同居させたウイルス非接種薬物非投与動物での感染性ウイルス量(感染フェレットから隔離後4日目)は検出限界未満であった。SARS-CoV-2感染シリアンハムスターモデルでは、モルヌピラビルは肺でのウイルスRNA及び感染性ウイルス量を減少させた。感染後に摘出した肺組織の病理組織学的検査で、媒体群と比較してモルヌピラビル群ではSARS-CoV-2のウイルス抗原量の低下及び肺病変の軽減が認められた。
- 薬剤耐性:細胞培養系でのSARS-CoV-2のNHCに対する耐性の誘導については検討していない。他のコロナウイルス(MERS-CoV)を用いた耐性誘導試験では、細胞培養系で30回継代した結果、2倍程度の感受性の低下が認められた。この30回継代したMERS-CoVではゲノム全体にランダムに変異が認められた。
モヌルピラビルはプロドラックで、体内でNHC(N-ヒドロキシシチジン)に分解されて細胞内に取り込まれてNHC-TPという物質になり、NHC-TPがウイルスに取り込まれることで、作用を発揮するようです。
in vitroの結果では従来株および変異株(α、β、γ、δ)への抗ウイルス効果は同程度のようです。
今流行しているオミクロン株についての情報はありませんが、コロナウイルスのウイルス由来RNA依存性RNAポリメラーゼが変異株のなかでも同等であれば、効果は発揮しそうです。
また、他のコロナウイルス(COVID-19ではないもの)で30回継代したものは2倍程度の感受性低下、ゲノム全体にランダムに変異が認められたとあるので、将来的には耐性ウイルスができる可能性があるようです。
臨床試験情報
中間解析の主要評価項目の結果として添付文書に次の表が記載されています。
| モヌルピラビル800mg群 (385例)例数(%) | プラセボ群 (377例)例数(%) | 割合の群間差 (95%信頼区間) | P値 | |
| 無作為化29日目までの理由を問わない すべての入院または死亡 | 28 (7.3%) | 53 (14.1%) | -6.8 (-11.3、-2.4) | 0.0012 |
| 入院 | 28 (7.3%) | 52 (13.8%) | ||
| 死亡 | 0(0%) | 8(2.1%) | ||
| 不明 | 0(0%) | 1(0.3%) |
以前ご紹介した全症例の結果の表は 経口コロナ治療薬 モルヌピラビルについて調べてみました | りんブログ (lynn-pharma.com) で紹介したものです。
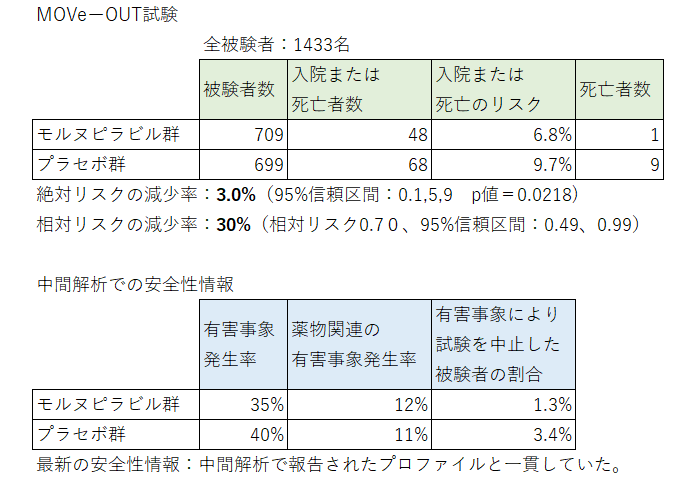
すべての人が入院しない、というわけではありませんが、プラセボよりは入院まで至る割合が抑えられており、重症化する前に治療できそうです。内服薬で効果が出るのはありがたいですね。
効能効果 用法用量
ラゲブリオカプセルは赤茶色のカプセルで中にRNAポリメラーゼ阻害薬であるモヌルピラビルが200㎎入っています。効能効果、服用方法は次の通りです。
- 効能または効果:SARS-Cov-2による感染症
- 効能効果に関する注意
- 重症化リスク因子を有する等、本剤の投与が必要と考える患者に投与
- 重症度の高いSARE-Cov-2による感染症患者に対する有効性は確立していない
- 効能効果に関する注意
- 用法及び用量:通常、18歳以上の患者には、モヌルピラビルとして1回800㎎(4カプセル)1日2回5日間経口投与する。
- 用法用量に関する注意
- SARE-Cov-2による感染症の症状が発現していから速やかに投与を開始すること
- 臨床試験において、症状発現から6日目以降に投与を開始した患者における有効性を裏付けるデータは得られていない。
- 用法用量に関する注意
ラゲブリオカプセルの投与対象としては、軽症~中等症Ⅰの重症化リスク因子を有する18歳以上が対象となるようです。
重症化リスク因子は以下の通りです。
- 61歳以上
- 活動性のがん(免疫抑制または高い死亡率を伴わないがんは除外)
- 慢性腎臓病
- 慢性閉塞性肺疾患
- 肥満(BMI30kg/m2以上)
- 重篤な心疾患(心不全、冠動脈疾患または心筋症)
- 糖尿病
使用対象者に対する注意
禁忌(次の患者には投与しないこと)には、本剤成分の過敏症既往歴および妊婦または妊娠している可能性のある女性とあります。
添付文書上には、生殖能をゆうする者、妊婦、授乳婦、小児等、特定の背景を有する患者(腎機能障碍者、肝機能障害者、高齢者)について記載があります。
- 生殖能を有する者:妊娠可能な女性に対しては、本剤投与中及び最終投与後一定期間は適切な避妊を行うよう指導すること。
- 妊婦:妊婦又は妊娠している可能性のある女性には投与しないこと。
- 動物実験で胎児毒性が報告されている。
- 妊娠ラットの器官形成期にモルヌピラビルを投与した実験において、N-ヒドロキシシチジン(NHC)の臨床曝露量の8倍に相当する用量で催奇形性及び胚・胎児致死が、3倍以上に相当する用量で胎児の発育遅延が認められている。
- また、妊娠ウサギの器官形成期にモルヌピラビルを投与した実験において、NHCの臨床曝露量の18倍に相当する用量で胎児体重の低値が認められている。
- 授乳婦:治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。動物において、モルヌピラビルの乳汁移行試験は実施しておらず、ヒト乳汁中への移行の有無及び乳汁産生への影響に関するデータはない。
- 小児等:18歳未満を対象とした臨床試験は実施していない。
- 腎機能障害者:モルヌピラビル及びNHCの主要な消失経路は腎排泄ではないため、腎機能障害がこれらの排泄に影響を及ぼす可能性は低い。母集団薬物動態解析の結果、軽度及び中等度の腎機能障害がNHCの薬物動態に及ぼす意味のある影響はみられなかった(外国人データ)。重度腎機能障害患者(eGFR 30mL/min/1.73m2未満)又は透析を必要とする患者におけるモルヌピラビル及びNHCの薬物動態の評価は実施していない.
- 肝機能障害者:肝機能障害者におけるモルヌピラビル及びNHCの薬物動態の評価は実施していない。非臨床試験の結果、NHCの主要な消失経路は肝代謝ではないと考えられた。また、モルヌピラビルは主に消化管及び肝臓でNHCへ代謝される一方、モルヌピラビルの加水分解に必要な代謝酵素は広範な組織に分布しているため、肝機能障害がモルヌピラビル及びNHCの曝露量に影響を及ぼす可能性は低い。
- 高齢者:母集団薬物動態解析の結果、高齢者におけるNHCの薬物動態は若年者と同様であった。
ラゲブリオカプセルは、妊婦・妊娠している可能性のある女性には使用できないこと、小児は使用対象外(臨床試験実施なし)であること以外は特に影響はなさそうです。授乳婦については乳汁移行試験をしていないので、本人や医師の判断となります。
副作用
臨床試験での副作用(有害事象のうち因果関係が否定できないもの)は次の通りです。
| 1%以上5%未満 | 1%未満 | 頻度不明 | |
| 胃腸障害 | 下痢、悪心 | 嘔吐 | |
| 神経系障害 | 浮動性めまい、頭痛 | ||
| 皮膚及び皮下組織障害 | 発疹、蕁麻疹 | 中毒性皮疹 |
皮疹への注意は必要ですが、あとは大きな影響はなさそうです。
まとめ
ラゲブリオカプセルはCOVID-19の軽症の方に投与できる内服薬として、重症化因子をもつ18歳以上に対して今後使われていくと思います。
オミクロン株への効果は不明であり、今後のデータに期待です。


コメント